牛津大學研究揭開高血糖如何導致2型糖尿病的謎團
(神秘的地球uux.cn)據cnBeta:牛津大學的一個研究小組揭開了高血糖究竟如何導致2型糖尿病的謎團。這一發現顯示,葡萄糖代謝物可以損害胰腺β細胞,導致2型糖尿病的發展,而破壞這一過程可以提供一種治療該疾病的新方法。
國際糖尿病聯盟估計目前全世界有超過5億人患有糖尿病,其中絕大多數人患有2型糖尿病。這種疾病的特點是高血糖,即血液中循環的葡萄糖含量高。
研究人員早就知道,2型糖尿病主要是飲食不當和缺乏運動的結果。長期的高糖消費通過破壞身體釋放胰島素的能力而導致2型糖尿病,胰島素是一種已知的降低血糖水平的荷爾蒙。
研究人員還沒有清楚地了解的是,長期的高血糖水平究竟是如何損害我們產生胰島素的β細胞。新研究的主要研究人員之一Elizabeth Haythorne之前已經確定,慢性高血糖會損害β細胞,所以下一步是要弄清楚這種損害到底是如何發生的。
Haythorne解釋說:"我們意識到,我們接下來需要了解葡萄糖是如何損害β細胞功能的,因此我們可以考慮如何阻止它,從而減緩T2D中β細胞功能似乎不可阻擋的下降。"
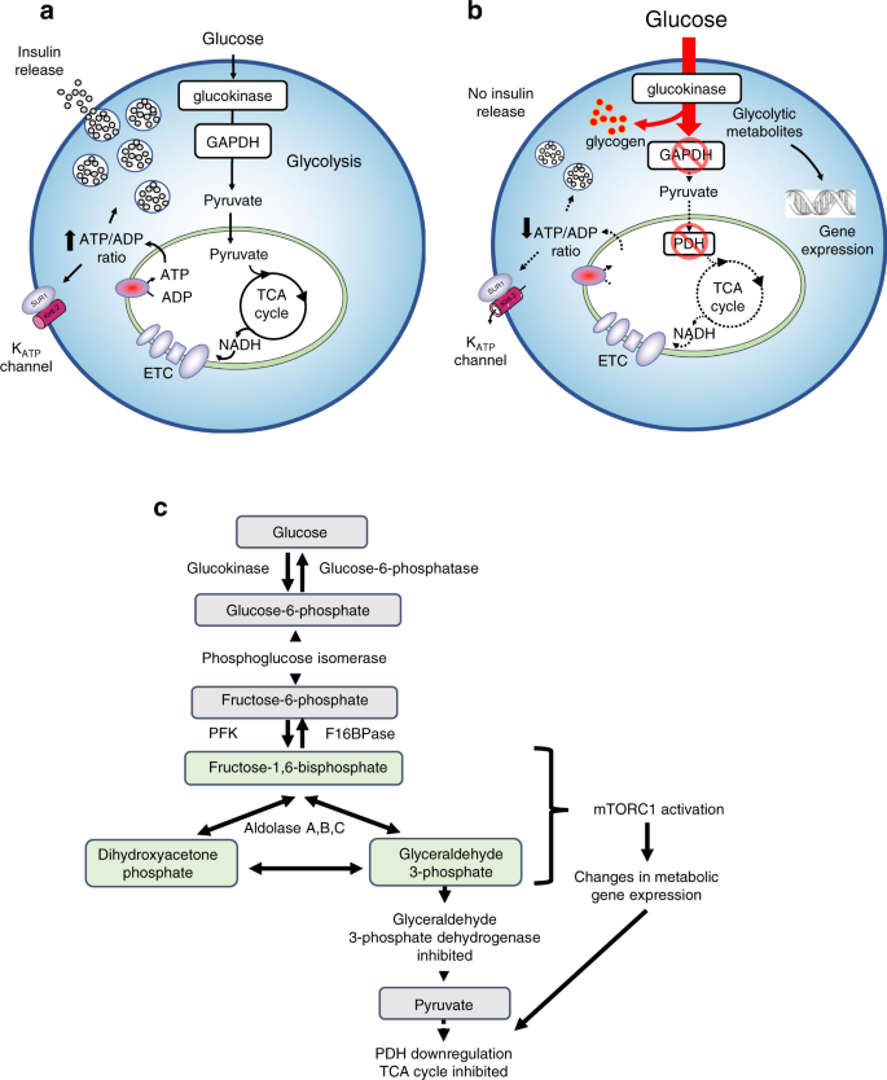
在一係列的動物研究和培養細胞調查中,研究人員發現,損害胰島素分泌β細胞功能的不是葡萄糖本身,而是通過葡萄糖代謝過程中產生的產品。研究人員仍不清楚到底是什麽具體的葡萄糖代謝物觸發了這一過程,但它們確實清楚地表明,即使在高血糖水平下,抑製葡萄糖的代謝也能維持胰島素的分泌。
有趣的是,這一發現有些反直覺,研究人員發現,通過抑製一種叫做葡萄糖激酶的酶,阻斷葡萄糖代謝過程,實際上改善了動物的胰島素分泌。從事這項研究的另一位研究員弗朗西斯-阿什克羅夫特說,這一發現與以前試行的治療2型糖尿病(T2D)的方法相反。
"因為葡萄糖代謝通常會刺激胰島素分泌,所以以前假設增加葡萄糖代謝會增強T2D的胰島素分泌,葡萄糖激酶激活劑被試用,結果各不相同,"Ashcroft指出。"我們的數據表明,葡萄糖激酶激活劑可能有不利影響,而且有點反直覺的是,葡萄糖激酶抑製劑可能是治療T2D的更好策略。"
研究人員強調這些發現仍然是非常初步的,所以在這種治療方法進入臨床使用之前還需要大量的工作。但這一具有裏程碑意義的發現確實重塑了我們對開發治療2型糖尿病新方法的思考。這表明存在一種潛在的方法,可以減緩或防止T2D中β細胞功能的下降。
這項新研究發表在《自然通訊》上。
相關:日本研究人員對導致糖尿病的機製有了新的認識
(神秘的地球uux.cn)據cnBeta:科學家們發現T-鈣粘素是一種將胰島素缺乏反饋給胰腺β細胞並誘導其增殖的因素,有可能用於治療糖尿病。由日本大阪大學領導的研究人員現在已經確定了一種機製,通過這種機製,胰島素的缺乏可能被反饋給產生胰島素的胰腺細胞。這一發現為糖尿病提供了一個潛在的新治療目標。
研究人員發現了一種機製,通過這種機製,胰島素的缺乏可能被反饋給產生胰島素的胰腺細胞,確定了一個潛在的糖尿病新治療目標。
據估計,全世界有超過4億人患有2型糖尿病,盡管如此普遍,體內的胰島素調節機製仍然沒有得到充分的了解。
當胰腺無法提供足夠的胰島素時,就會發生2型糖尿病。胰島素是控製糖的使用和儲存的激素,以滿足生理需求。如果身體對胰島素的需求得不到滿足,胰腺中製造胰島素的細胞,即所謂的β細胞,通常可以增殖以增加其數量。然而,目前還不知道是什麽因素從接受胰島素的組織或細胞中釋放出來,向胰腺β細胞發出缺乏胰島素的信號。
在11月7日發表在《科學》雜誌上的一項研究中,科學家們發現一種名為T-鈣粘素的分子可能參與向胰島素分泌的胰腺細胞提供反饋並控製其增殖。T-鈣粘素通常存在於細胞表麵,並且最著名的是作為一種叫做adiponectin的分子的結合夥伴--一種專門由儲存脂肪的細胞分泌的因子。
然而,研究人員表明,T-鈣粘素也以以前未描述的可溶性形式分泌,並能作為一種體液因子發揮作用,即通過循環係統運輸的分子。他們不僅認識到T-鈣粘素對胰島素缺乏有反應,而且還證明了經過基因工程設計的缺乏T-鈣粘素的小鼠在用高脂肪飲食喂養時有葡萄糖耐量受損。
"用於調查全基因組基因表達水平的RNA測序分析顯示,缺乏T-鈣粘素的小鼠β細胞中Notch信號蛋白的表達減少,"主要作者Tomonori Okita和通訊作者Shunbun Kita解釋說。這些蛋白在被認為促進β細胞增殖的Notch信號通路中發揮作用;這表明可溶性T-鈣粘素通過Notch通路向胰腺β細胞發出信號以增加胰島素的生產。
"我們然後用人工合成的T-鈣粘素來處理分離的小鼠胰島,這是包含β細胞的胰腺部分"高級作者Iichiro Shimomura解釋說。"這種處理方法促進了小鼠胰島中的Notch信號,這反過來又能誘導β細胞的增殖"。令人興奮的是,這些發現表明,T-鈣粘素可以應用於糖尿病的根本治療。
相關:討厭針頭?糖尿病和癌症患者可能可以告別頻繁注射藥物了
(神秘的地球uux.cn)據cnBeta:加州大學河濱分校(UCR)的科學家們正在為糖尿病和癌症患者尋找出路,讓他們忘記針頭和頻繁的注射。相反,這些病人將能夠服用藥丸來控製他們的病情。治療這些疾病的一些藥物會溶解在水中。這意味著通過腸道運輸這些藥物是不可行的,因為腸道也處理我們的飲料和食物。因此,這些藥物不能有效地通過口服給藥,即通過口腔吞咽藥物。
然而,加州大學洛杉磯分校的科學家們已經創造了一種化學"標簽",可以添加到這些藥物中,從而使它們通過腸道進入血液循環。
在最近發表在《美國化學學會雜誌》上的一篇新論文中,研究人員詳細介紹了他們如何發現這種標簽並證明其有效性。
該標簽由一個小肽組成,它就像一個蛋白質片段。"因為它們是相對較小的分子,你可以用化學方法將它們附著在藥物,或其他感興趣的分子上,用它們來口服這些藥物,"領導這項研究的UCR化學教授Min Xue說。
當研究人員觀察到這些肽進入細胞時,Xue的實驗室正在測試一些無關的東西。"我們沒有想到會發現這種肽會進入細胞。這讓我們大吃一驚,"Xue說。"我們一直想找到這種化學標簽,而它最終偶然地發生了。
Xue說,這一觀察是出乎意料的,因為以前,研究人員認為這種類型的傳遞標簽需要攜帶正電荷才能被帶負電的細胞接受。他們對這種名為EPP6的中性肽標簽的研究表明,這種想法並不準確。
在測試這種肽在體內移動的能力時,Xue小組與南加州大學凱克醫學院的Kai Chen小組合作,將這種肽喂給小鼠。使用PET掃描--一種類似於南加州大學提供的全身X射線的技術,該小組觀察到肽在腸道中的積累,並記錄了其最終通過血液轉移到動物的器官中。
PET掃描圖像顯示,口服EPP6在腸道中積累,並通過血液循環進入大腦和膀胱。資料來源:Min Xue/UCR
在證明了該標簽通過口服成功地在循環係統中導航後,該團隊現在計劃證明該標簽在附著於一些藥物時也能做同樣的事情。Xue說:"相當有說服力的初步結果使我們認為我們可以進一步推動這項工作。"
許多藥物,包括胰島素都必須注射。研究人員希望他們的下一組實驗將改變這種情況,使他們能夠將這種標簽添加到各種各樣的藥物和化學品中,改變這些分子在體內移動的方式。這一發現可以為那些已經被疾病所困擾的人解除負擔。










